中国科学院广州生物医药与健康研究院刘劲松课题组通过结构生物学研究,在分选转运蛋白(SNXs)中发现了一类新型的非典型G 蛋白信号转导调节因子(RGS)同源结构域(RGS homology,RH)。相关工作近日以Structural studies reveal unique non-canonical regulators of G protein signaling homology (RH) domains in sorting nexins为题在Journal of molecular biology上在线发表。
作为内吞途径的第一个转运分选站,内涵体被认为是信号转导的重要平台。越来越多的研究发现,很多被内吞的G蛋白偶联受体(GPCR),在内涵体上依然具有信号转导活性。由于含有RGS 同源结构域(RH),SNX-RH亚家族蛋白(SNX13、SNX14和SNX25)被认为可能具有分选转运和调控GPCR-G蛋白信号转导的双重功能。然而,科学家们对SNX-RH蛋白的RH结构域是否具有G蛋白信号转导调节活性仍然存在争议。
为了更好的认识SNX-RH蛋白RH结构域的功能,课题组对SNX-RH蛋白的RH结构域进行了结构生物学研究。课题组获得了SNX13、SNX14和SNX25的RH结构域的晶体,并成功解析了SNX13-RH和SNX25-RH结构域的晶体结构。通过结构分析和Co-IP实验,课题组发现这两个RH结构域都能形成同源二聚体。进一步分析发现,SNX-RH蛋白的RH结构域都缺乏结合Gα蛋白的关键氨基酸。Co-IP实验和生物膜干涉实验都表明,SNX13、SNX14和SNX25的RH结构域都不能结合Gα蛋白。因此,课题组推测SNX13、SNX14和SNX25的RH结构域不具有G 蛋白信号转导调节活性,而是可能发挥二聚体模块的功能,介导SNX-RH蛋白形成寡聚体。
本研究为SNX-RH亚家族蛋白的功能机制研究提供了结构基础。
广州健康院博士生张玉龙为第一作者,徐进新副研究员和刘劲松研究员为共同通讯作者。该研究获得了国家自然科学基金、中科院青促会和呼吸疾病国家重点实验室等单位项目的支持。
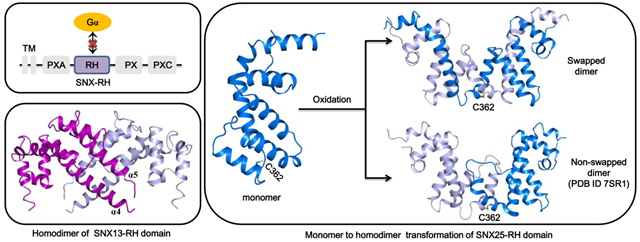
SNX13和SNX25RH结构域的晶体结构及同源二聚体的形成
附件下载:


