近日,中国科学院南海海洋研究所张长生研究员团队在抗性基因介导海洋微生物天然产物结构多样化研究中获得新进展。研究揭示了糖苷酶KijX水解海洋微生物天然产物Lobophorin(LOBs)中的糖基侧链,从而介导菌株对LOBs产生抗性的新机制,阐明了异源重组菌株中LOBs的结构多样化是内源基因和外源基因簇间相互作用的结果,为抗生素耐药性和结构多样化研究提供了新思路。相关研究成果“A Widespread Glycosidase Confers Lobophorin Resistance and Host-Dependent Structural Diversity”发表于Angewandte Chemie International Edition (《德国应用化学》),并被遴选为”Hot Paper"。
抗生素耐药问题正在引发全球健康危机,普遍认为耐药性的产生与抗生素的广泛使用息息相关。但越来越多的研究发现,即使在人迹罕至的冻土和洞穴中发现的微生物中也存在抗生素抗性基因,表明环境微生物作为抗性基因的储存库,可能是临床耐药菌株中抗性因子的起源。这也提出了一个关于抗生素与其抗性基因演化过程中“先有鸡还是先有蛋”的有趣问题:是抗生素的广泛使用催生了抗性基因的进化,还是抗性基因本已古老存在,只是因抗生素的使用而加速了其发现过程?无论如何,从环境微生物中鉴别新的抗生素抗性基因,理解其生态功能,可以为抗生素的临床耐药性提供潜在的可控措施和解决方案。
LOBs属于螺环乙酰乙酸内酯类抗生素,研究人员前期从海洋来源链霉菌Streptomyces sp. SCSIO 01127中分离到LOBs A/B,解析了LOBs生物合成中负责糖基化(LobG1、LobG2和LobG3)(Org Lett, 2013, 15, 1374-1377; Org Lett, 2020, 22, 1062-1066)、糖甲基化(LobS1)(Appl Microbiol Biotechnol, 2013, 97, 3885-3892)和C-32羟化(LobP1)(Chin J Chem, 2023, 41, 1478-1484)等后修饰酶的功能(图1)。但在近期研究中发现一个特别的现象:与野生型菌株产物不同,异源重组菌株S. coelicolor M1154/pCSG5560(含有lob基因簇)中产生了一系列C-9位带单糖且C-32位为羟甲基的LOBs,而意外的是,虽然LobP1体外反应确证其负责C-9位带三糖或双糖的LOBs的C-32位甲基羟化,但LobP1却不能催化C-9位带有单糖的LOBs发生羟化(图1)。由此产生了异源重组菌株中这些C-9位带单糖且C-32位为羟甲基的LOBs是如何产生的问题。
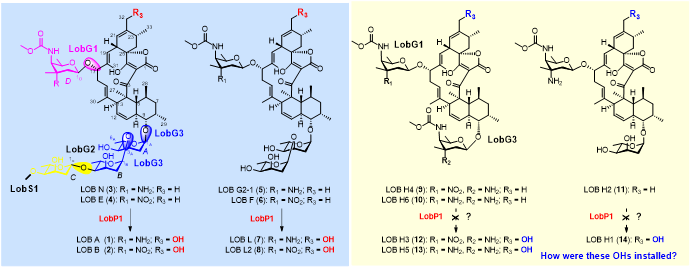
图1. 野生型菌株(浅蓝色)和异源表达菌株(浅黄色)中产生的代表性LOBs及部分后修饰酶的功能
基于上述问题,通过文献调研和生物转化实验,研究人员在异源宿主中发现了一个糖苷酶KijX,可催化LOBs中C-9位多糖链的水解,但不能催化C-9位带单糖的LOBs发生糖基水解(图1)。在异源重组菌株S. coelicolor M1154/pCSG5560中,LOBs的合成经历了LobG1(C-17糖基化),LobG3(C-9位连续添加两个糖)和LobG2(C-9位的第三个糖)催化的糖基化,KijX催化的C-9位三糖(或双糖)产物脱糖,LobG3催化的C-9位重新糖基化(单糖)的复杂过程(图2)。通过外源基因簇lob和内源基因kijX之间相互作用,最终实现了LOBs的结构多样化。
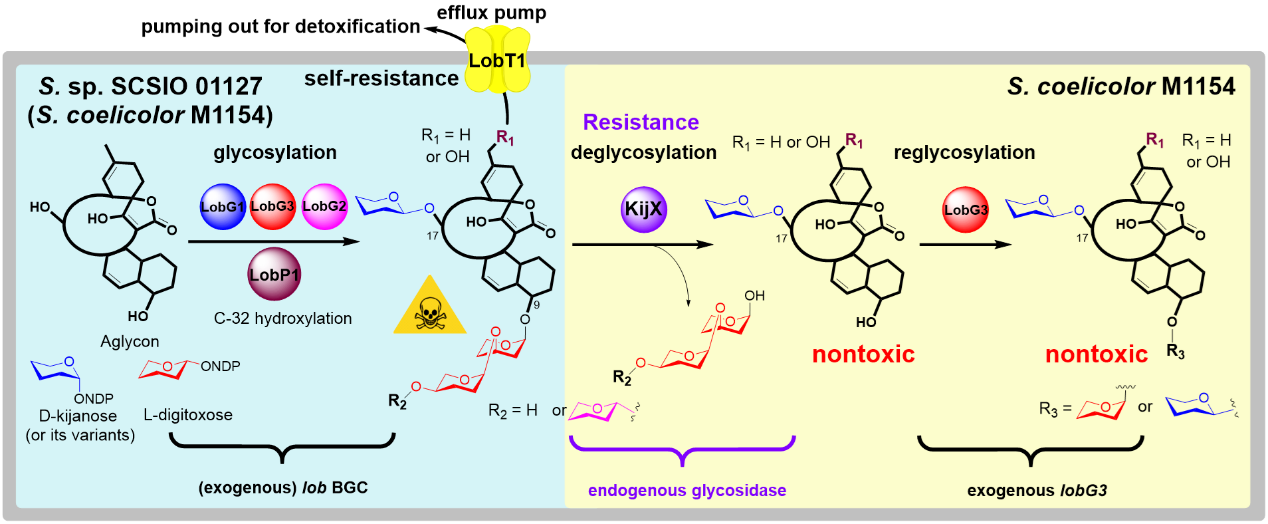
图2.野生型菌株和异源重组菌株中LOBs产生的差异及菌株对LOBs产生抗性的分子机制
进一步的生物信息学分析发现,KijX的同源酶在细菌、真菌和古菌中广泛存在。查询到细菌来源KijX蛋白2323个,真核生物来源68个,古菌来源9个。体外酶学实验显示,在选取的56个不同来源的KijX同源蛋白(相似性28?91%)中51个有水解糖基的活性,部分同源蛋白的活性优于KijX。由于KijX同源蛋白广泛存在于放线菌门中,推测该酶可能为放线菌对抗环境中LOBs的一种抗性机制。活性评价实验显示C-9位带有单糖或无糖的LOBs对放线菌指示菌株没有抑制活性;C-9位带有三糖或双糖的LOBs能够抑制不含kijX及同源酶基因的放线菌的生长。导入kijX基因后,敏感菌株对LOBs产生抗性。相反,C-9位带有三糖或双糖的LOBs不能抑制含有kijX及同源基因的放线菌的生长,但敲除kijX及同源基因后,菌株对LOBs敏感(图3)。这些实验证实了kijX及其同源基因为LOBs的抗性基因。菌株间的拮抗实验显示同样的结果,表明菌株通过产生LOBs来抑制同一生境中其他微生物的生长以获得竞争优势,体现了环境微生物间的一种共进化关系(图3)。

图3. kijX作为抗性基因的鉴定以及LOBs产生菌和非产生菌之间的拮抗作用
为了进一步阐明这类特殊糖苷酶的作用机制,研究人员解析了AcvX(KijX同源蛋白)的晶体结构。与AlphaFold2预测的15个其他KijX同源蛋白结构比较显示,这类酶含有典型的GH113家族糖基水解酶的(β/α)8桶状结构,但与典型GH113家族水解酶相比,KijX及其同源酶与底物结合的口袋呈现出特征的带负电的凹槽,这个负电凹槽是该类酶特异性对LOBs产生水解作用的关键结构特征。进一步通过晶体叠加和点突变分析找到了该类蛋白可能的催化位点,并推测了其催化机制。
绝大多数KijX同源酶在本研究之前被注释为未知功能蛋白,含有kijX的微生物在环境中分布非常广泛,涵盖了沙漠、海洋和深洞,以及人体和动物的肠道微生物。与此相反,含有LOB生物合成基因簇的微生物大多数来自于海洋环境。由此推测某些抗生素的抗性基因本已古老存在,抗生素的广泛使用加速了其发现过程。kijX及其同源基因作为LOBs的抗性基因是巧合还是必然,是否其进化的目的是为抵抗环境中的LOBs均还未知,它们的原始生物学功能还有待进一步研究。
谭彬博士、张丽萍副研究员和张庆波研究员为本文共同第一作者,朱义广和张长生研究员为共同通讯作者。该研究得到了国家重点研发计划项目、国家自然科学基金重大项目、广东省海洋经济发展(海洋六大产业)专项资金项目、海南省重大科技计划项目和中国科学院王宽诚率先人才计划“卢嘉锡国际团队项目”等资助。
相关论文信息:
A Widespread Glycosidase Confers Lobophorin Resistance and Host-Dependent Structural Diversity. https://doi.org/10.1002/anie.202302043
附件下载:


