近日,中国科学院广州生物医药与健康研究院赖良学课题组在基因蛋白表达水平的双向定量调控领域取得了重要突破。相关成果以“Precise genome editing of the Kozak sequence enables bidirectional and quantitative modulation of protein translation to anticipated levels without affecting transcription”为题在线发表于Nucleic Acids Research(核酸研究)杂志。该研究以蛋白翻译调控元件—Kozak序列为切入点,开发出一种全新的、普适的策略,用于精细调控目标基因蛋白表达水平。这种策略在不触及基因转录的情况下,既能实现蛋白表达水平的双向(上调或下调)调控,又能将蛋白表达水平控制在预测范围内。
基因的表达包括转录和翻译两个过程,其表达水平的调控可以在多个层面上进行,包括基因组、转录、翻译等层面。过去的研究已经对调控基因表达进行了大量探索,并取得了许多重要的进展。例如,通过使用基因编辑工具对基因序列进行编辑,引入移码突变或破坏起始密码子等,可以实现目标基因的完全敲除;利用组成型启动子或组织特异性启动子,可以实现目标基因的过量表达;利用RNA干扰技术或CRISPR/Cas9激活或抑制系统,可以实现目标基因的激活或抑制。然而,这些策略只能实现目标基因的完全敲除或将目标基因的表达量调控到不可预测的水平,而不能实现目标基因的可预测定量调控。
在真核细胞的mRNA中,非翻译区(Untranslated Region,UTR)存在调控基因翻译的元件,如Kozak序列、上游开放阅读框(Upstream Open Reading Frame, uORF)等。有课题组针对uORF进行设计,建立了精细上调或下调内源基因翻译的方法,并成功应用到植物分子设计育种领域。但该策略无法定量地将蛋白表达控制在特定水平。Kozak序列是翻译起始附近的序列,对于核糖体正确识别翻译起始密码子具有直接关系,其序列的不同,会导致蛋白合成量的差异,这提示了通过改造基因Kozak序列可能获得不同翻译效率的调控效果。
因此,该研究基于对编码基因Kozak序列的精确操作,提出了一种名为KZ3-edit的新型基因表达调控策略:利用精准基因编辑技术在DNA水平上精确修饰起始密码子上游的3个核苷酸(这是Kozak序列的一部分,碱基偏好最显著,被命名为KZ3),这足以高效调控基因的翻译效率。在不改变基因的转录水平和蛋白质序列的情况下,对mRNA的翻译水平进行定量和双向调控,从而将蛋白表达精细地控制在预期的水平。通过体外双荧光报告系统、绿色荧光细胞系及内源基因三个层面,研究人员验证了KZ3-edit策略的有效性和灵活性,并证实通过精准基因编辑工具对基因主效开放阅读框(Primary Open Reading Frame, pORF)或uORF起始密码子上游KZ3序列的单个碱基改变或碱基组合转变,可以实现特定基因翻译水平的高效调控。
此外,研究人员还将该策略应用于家兔生物性状的调控,分别以调节脂质代谢的PCSK9基因和调控毛发生长周期的HR基因为靶基因。一方面,通过改变PCSK9基因的pORF的KZ3序列来直接降低PCSK9蛋白表达量,成功构建了低胆固醇家兔模型;另一方面,通过修饰HR基因的uORF—U2HR,改变其KZ3序列而间接上调HR基因的蛋白表达量,成功构建了遗传性少毛症家兔模型。这两种家兔模型的成功构建为KZ3-edit策略在基因的精细调控中的应用,以获得目标生物性状提供了范例。
该研究提出了一种普适、高效、灵活的基因翻译调控新策略,可以对目标基因起始密码子前三个碱基进行直接基因编辑,从而实现双向定量调控目标基因翻译水平的效果。这种策略理论上可以应用于真核生物所有的编码基因,且该策略调控翻译的有效性、设计简便性以及应用多样性将为基因功能研究、人类遗传疾病模型构建与治疗、农业精准分子设计育种等提供重要的技术手段。
本研究中,广州健康院谢精科副研究员、庄镇鹏博士和苟士学博士为共同第一作者,王可品研究员和赖良学研究员为共同通讯作者。该研究成果得到了国家重点研发计划、国家自然科学基金、海南省科技计划、广东省科技计划、中国科学院青年创新促进会等项目的资助。
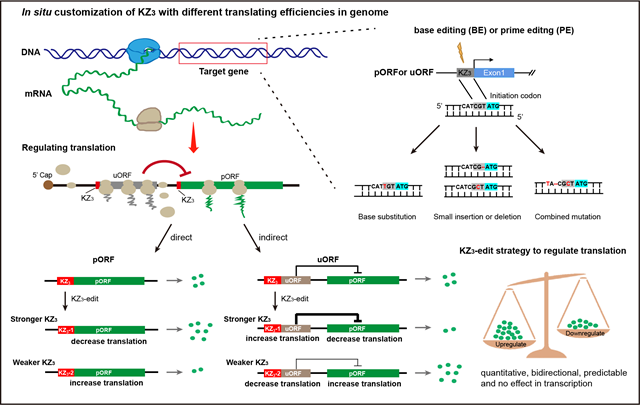
KZ3-edit策略原理图
附件下载:


