近日,中国科学院广州生物医药与健康研究院等单位合作在Nature Microbiology发表题为SARS-CoV-2 Delta and Omicron variants evade population antibody response by mutations in a single spike epitope的研究论文。
该研究发现一株靶向病毒蛋白受体结合域(RBD)半隐藏表位并具有高亲和力的人源中和抗体R1-32,主要通过打开刺突蛋白并将其瓦解的方式阻止病毒进入细胞;抗体组库分析显示,由IGHV1-69编码的类R1-32抗体在新冠感染人群中被广泛诱导。这是继此前发现的新冠特异性IGHV3-53和IGHV1-58人群共享抗体谱系之后,被发现的又一类由IGHV1-69编码的新冠特异性人群公共性抗体谱系。该研究提供了证据,显示类R1-32抗体谱系特异性靶向L452位点可能是促使Delta和Omicron BA.4/BA.5在该位点发生突变的重要原因。
新冠肺炎疫情从2019年底爆发至今仍在全球持续蔓延,严重影响了人类健康及社会经济。在自然感染和疫苗接种建立的群体免疫压力作用下,SARS-CoV-2不断发现发生变异以逃避抗体的中和。尤其是目前在全球大流行的Omicron突变株的刺突蛋白携带超过30个位点的突变并持续演化。不断出现的突变株对疫苗和抗体药物的有效性造成了巨大的挑战。因此,阐明新突变株逃逸人群抗体的机制,对下一代疫苗及抗体药物的设计与开发具有重要意义。
围绕上述问题,本项研究运用多种技术手段,研究了从SARS-CoV-2早期感染者外周血B细胞中筛选获得的一株靶向RBD、非血管紧张素转化酶2(ACE2)竞争的高亲和力中和抗体R1-32。小鼠实验显示针对新冠病毒原始株感染,R1-32具有良好的保护效果。研究团队通过冷冻电镜解析获得了R1-32 Fab,ACE2与刺突蛋白三聚体三元复合物的高分辨率结构。结果显示,R1-32虽不阻碍ACE2受体结合,但通过靶向一个半隐藏表位破坏刺突蛋白结构,使刺突蛋白无法介导膜融合从而抑制病毒入侵细胞。进一步的结构分析显示,R1-32主要利用HCDR2和HCDR3与RBD发生相互作用,尤其是抗体IGHV1-69基因HCDR2编码的胚系疏水残基I52、I54、L55和I57与刺突蛋白上的疏水残基L452、F490和L492形成的疏水作用对于抗体识别抗原具有重要作用(图1)。 研究注意到L452,F490是新冠病毒刺突蛋白的突变热点,点突变实验进一步证实了L452和F490位点突变会显著影响R1-32与RBD的结合。病毒中和实验也证明R1-32能够被携带L452R的Delta突变株逃逸,最早涌现的高度突变的Omicron BA.1虽然并不逃逸R1-32,但是带有L452R突变的BA.4,BA.5变种迅速涌现,并在当下流行。
鉴于R1-32是利用IGHV1-69编码的胚系残基识别RBD,且关键识别部位为突变热点,研究团队运用了高通量抗体组库测序技术对类R1-32抗体在人群的分布情况进行了分析(图2)。结果发现,该类抗体在健康人群中的抗体组库中存在并可以IgM形式检测到,但是类R1-32抗体在新冠病毒感染后显著富集并主要以类别转换后的IgG形式存在。通过与新冠刺突蛋白特异性抗体数据库中的序列比对,研究发现类R1-32抗体在新冠病毒感染者及疫苗接种者中都被广泛诱导,提示IGHV1-69编码的类R1-32抗体是抗体群体免疫的重要组成部分,并很有可能是刺突蛋白452,490出现突变的主要免疫压力。
该研究鉴定了由IGHV1-69编码的一类新冠刺突蛋白特异性人群抗体的谱系,揭示了代表性抗体R1-32独特的表位特征与中和机制,并阐释了其对突变株的免疫选择压力,对下一代新冠疫苗及抗体药物的设计与评估具有重要意义。
本研究合作单位为生物岛实验室、广州医科大学、中国科学院武汉病毒研究所、广州国家实验室。广州健康院博士研究生何平、颜奇鸿,博士后刘邦慧,生物岛实验室高夕杰研究助理、武汉病毒所裴荣娟副研究员为本论文共同第一作者。 熊晓犁研究员、陈凌研究员、何俊研究员及陈新文研究员为本论文共同通讯作者。广州医科大学的赵金存教授团队对该研究中的动物实验提供了鼎力支持。
本研究得到国家自然科学基金项目、中国科学院战略性先导科技专项、广州市科学计划重点项目、广东省自然科学基金、呼吸疾病国家重点实验室自主项目、粤港澳呼吸系统传染病联合实验室项目、广东省钟南山医学基金的支持。
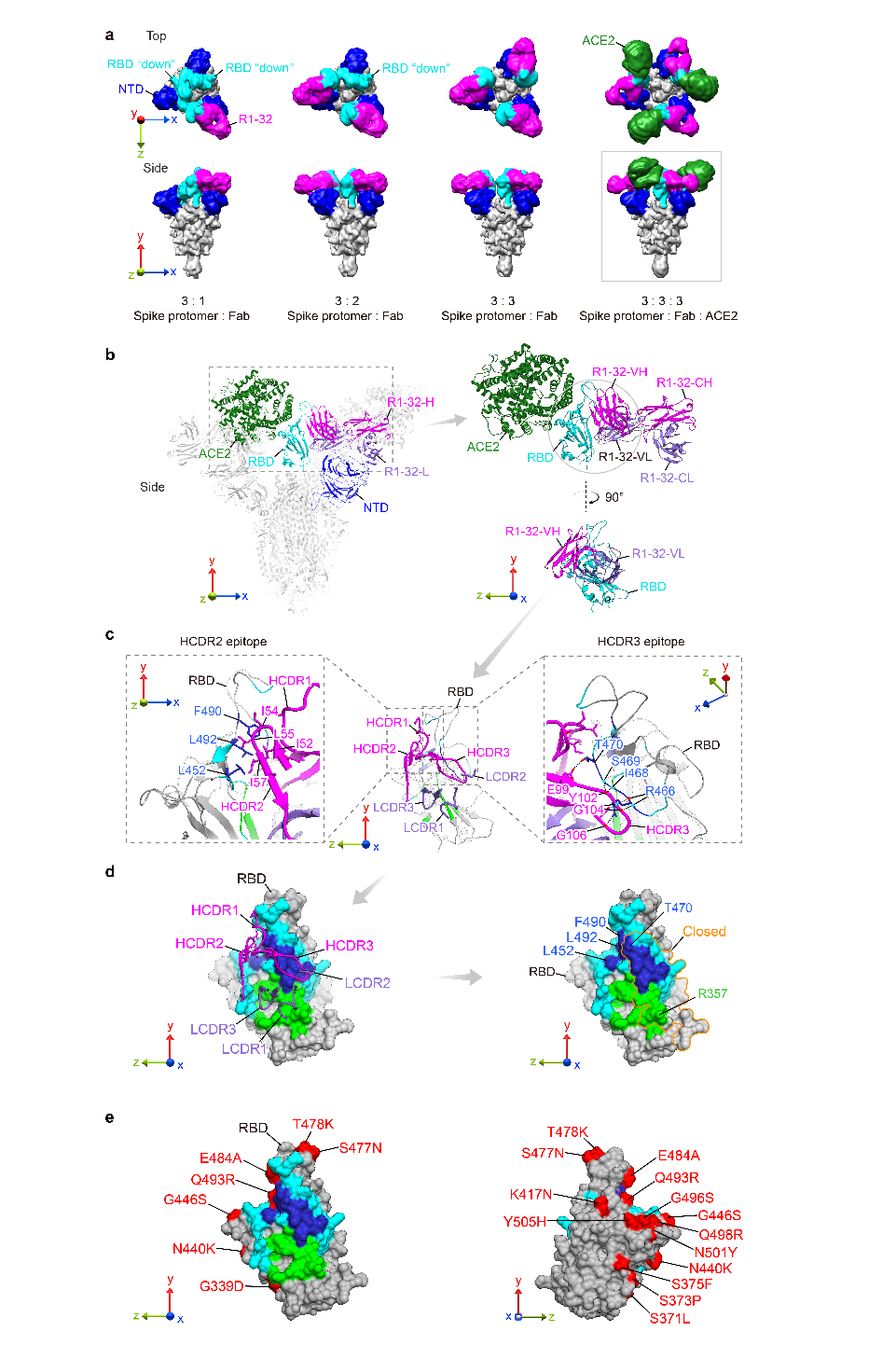
图1:R1-32与SARS-CoV-2刺突蛋白及R1-32表位结构图
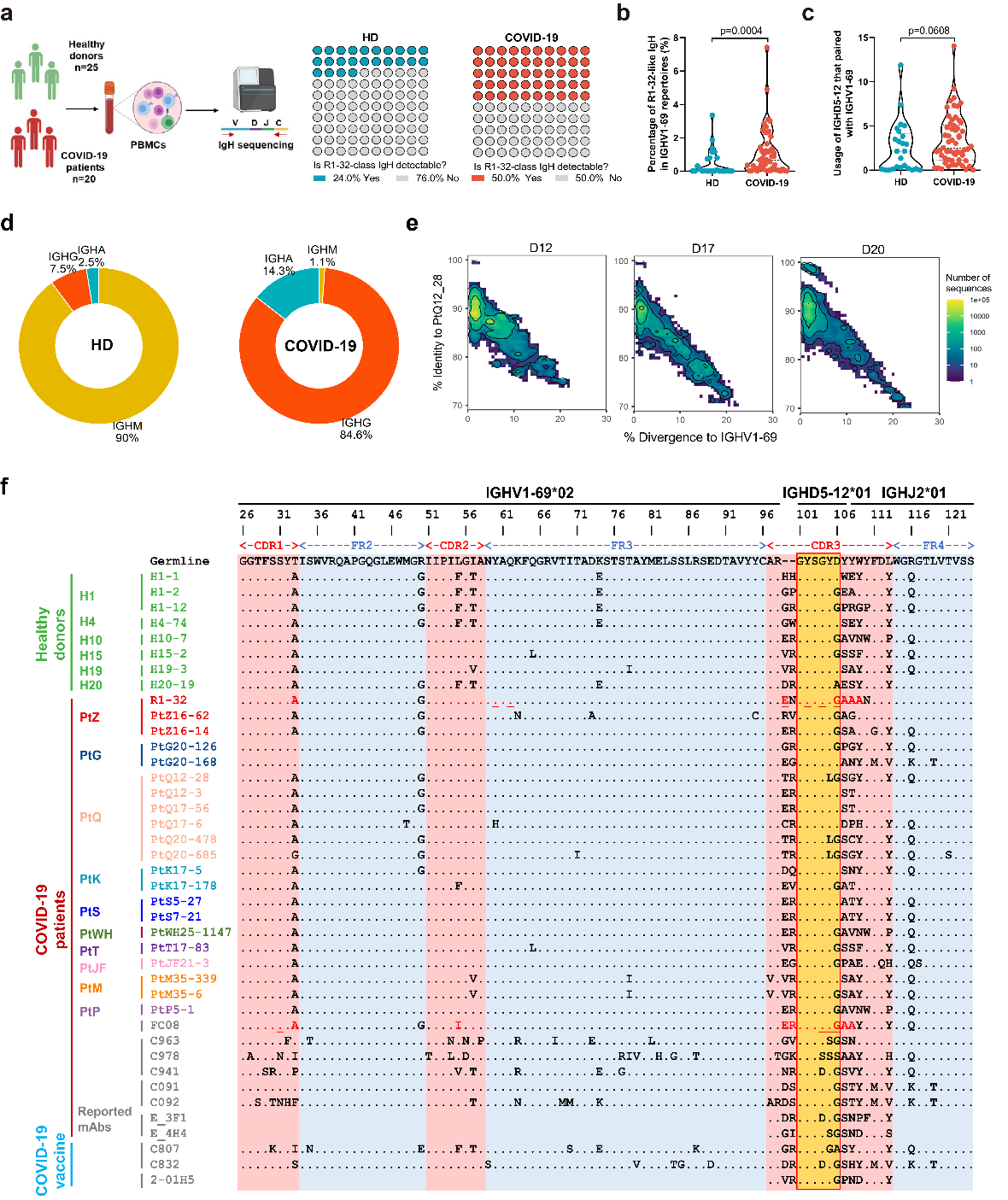
图2:R1-32类抗体在人群的广泛存在并COVID-19患者中快速诱导产生
附件下载:


